胃癌治療におけるオプジーボ(ニボルマブ)のまとめ

近年、抗がん剤の進歩は著しく、一昔前は太刀打ち出来なかったがんに対して新たな治療選択肢の開発がどんどん進んでいる。
現在、臨床試験(治験)中の薬剤も多く、がん全体で考えるとこれから怒涛の勢いで様々な薬が出てくる予定だ。
しかし、残念なことに、こと胃癌に関しては画期的な新薬の開発がほとんど進んでいないというのが実情だ。
ひとえに、
- 早期発見が比較的簡単で外科的に切り取った場合の予後が良好であること
- 抗がん剤に対する応答性が他の癌種に比べてあまり良くないこと
という特徴ゆえに、胃癌については早期癌の治療の進歩に重きが置かれ、進行癌患者は置き去りにされている感が否めない。
そんな胃癌ではあるが、最近の最大のトピックは、新薬としてニボルマブが進行胃癌治療に保険適用されたことだろう。
ニボルマブでピンとこない方もオプジーボと言えば聞き覚えがあるかと思う。
オプジーボ開発の原点となる研究成果が2018年のノーベル賞を受賞したことで連日大きく報道されたことは記憶に新しい。
ちなみに、ニボルマブは一般名でオプジーボは商品名のため、どちらも同じものを指す。
これまで置き去りにされてきたステージ4胃癌患者にとっては、久しぶりに得た新たな武器だ。
今回は、胃癌に対する治療薬としてのニボルマブの現況についてまとめたい。
ニボルマブについて
どんな薬

免疫チェックポイント阻害薬と呼ばれる薬剤であり、体内の免疫細胞をコントロールすることでがん細胞を排除し易くする薬だ。
一言で言ってしまえば抗体であり、PD-1というタンパク質に結合して作用を発揮する。
TS-1やシスプラチンのような古典的な抗がん剤は細胞そのものを傷害する薬剤だが、ニボルマブは直接がん細胞を攻撃する薬ではないため、基本的には癌の種類を選ばないというのが強み。
TS-1などの抗がん剤の解説はこちら。
一方、詳細は後述するが、副作用についても従来の抗がん剤では見られなかったようなものが生じることも明らかになっており、様々な面でこれまでにない新しい薬だと言える。
がんに作用する仕組み
そもそものPD-1の働き
PD-1は、リンパ球の1つであるT細胞を中心にB細胞やNK細胞などの免疫担当細胞の表面に存在するタンパク質であり、それらの細胞の働きを弱めるブレーキの役割を担っている。
本来、T細胞(厳密に言えば、細胞傷害性T細胞)は、病原体に感染した細胞を攻撃し、排除する働きを担っているため、その活性化は体を守るために必須だ。
一方で、活性化し過ぎると本来の攻撃対象ではない自分自身をも攻撃し始めてしまい、自己免疫疾患が生じてしまう。
それを防ぐため、人体の組織にはPD-L1やPD-L2というブレーキを押すためのタンパク質が存在しており、これらがT細胞の表面のPD-1と結合するとT細胞にブレーキがかかるという仕組みになっている。
このPD-1の発見に関して、京都大学の本庶 佑(ほんじょ たすく)先生が2018年のノーベル生理学・医学賞を受賞されたことでも大きな話題になった。
がん細胞とPD-1
そもそもがん細胞も細胞傷害性T細胞の攻撃対象であり、新たに発生したがんの多くは通常すぐに排除されている。
しかし、上述したT細胞のブレーキであるPD-1システムを悪用する一部のがん細胞、すなわちPD-L1を細胞表面に出したがん細胞は免疫からの攻撃を逃れることができるため、その細胞はどんどんと増殖していってしまう。
ニボルマブは、T細胞のPD-1に予め結合することで、がん細胞がかけようとするブレーキの邪魔をし、本来のT細胞が持つがんへの攻撃力を回復させ、抗がん作用を発揮する。
問題点
高い薬価
一時期大きな話題となったが、薬価が高すぎて引き下げられた経緯がある。
近年、様々ながんに適応が拡大しており、対象患者が増え続けているため、医療保険制度に与える影響が大きいと判断されたためだ。
元々は100mgで73万円だったが、2017年に半額の36.5万になった。
ちなみに今年(2018年)の4月にも値段が改定され、さらに下がるようだ。
2018年3月5日追記
100mgで27.8万(当初薬価から62%オフ)に改定される模様。
副作用
免疫のブレーキを解除する薬のため、副作用も従来のものとはかなり異なり、自己免疫を要因とする炎症性の副作用が特徴となる。
- 間質性肺炎
- 下痢・大腸炎
- 筋障害(重症筋無力症・心筋炎・横紋筋融解症)
- 肝機能障害
- 甲状腺機能障害
- 1型糖尿病
- 副腎機能障害
- 腎機能障害
などが代表的だが、程度の強弱を含めて何らかの副作用は80%程度の人に生じるとされる。
特に、間質性肺炎や重症筋無力症では死亡に至ったケースも報告されており、注意が必要な副作用だ。
胃癌治療におけるニボルマブの効果
どんな胃癌の人が対象か
化学療法(抗がん剤治療)を受け増悪した切除不能な進行または再発した胃癌患者が対象となっている。
つまり、早期癌患者は使うことができない。
さらに、標準治療の中の順番としては3次治療以降に位置付けられているので、進行胃癌患者の中でも従来の抗がん剤が2種類(レジメン)以上効かなくなってしまった人のみが対象となる。
進行胃癌に対する有効性
2017年のLancetに発表された進行胃癌患者を対象としたニボルマブの臨床試験の結果を紹介したい。
493人の進行胃癌患者がこの臨床試験に参加し、330人がニボルマブ、163人が偽薬の投与を受けた。
患者の生存期間の中央値は、ニボルマブ群では5.26ヶ月、偽薬群では4.14ヶ月だった。
この数字だけ見ると、僅か1.12ヶ月の差しかないため、その有効性を懸念される方もいるかもしれない。
しかし、長期生存の割合に目を向けると、ニボルマブ群では1年以上生存している人が26.2%なのに対して偽薬群では10.9%であり、大きな差がある。
さらに、がんの進行が止まっている期間で言えば、6ヶ月間がんの進行が止まったままの人は、ニボルマブ群が20.2%に対して偽薬群は6.8%、1年間となると、ニボルマブ群は7.6%に対して偽薬群は1.5%であった。
この臨床試験に参加している患者の80%は既に3種類以上の抗がん剤治療を受けてきた人であり、そのような厳しい背景でも効く人にはかなり効いている、という点で非常に画期的だろう。
副作用について
グレード3(重症)または4(生命を脅かす)の副作用がニボルマブ群では10.3%、偽薬群では4.3%で生じている。
1%を超える重大なものとして、
- 間質性肺炎(2.1%)
- 横紋筋融解症 (2.7%)
- 大腸炎・重度の下痢 (1.2%)
- 肝機能障害 (5.5%)
- 甲状腺機能障害 (3.9%)
- 神経障害 (3.0%)
が報告されている。
重症筋肉無力症や心筋炎などは認められなかったようだ。
今後の胃癌治療におけるニボルマブの位置付け
現在のところニボルマブは進行胃癌の3次治療からの使用に限られている上に、他の薬剤との併用は認められていない。
ただ、ニボルマブと他の免疫チェックポイント阻害薬や抗がん剤との併用により治療効果が高まることは既に他のがんで知られており、特定の肺癌や腎細胞癌では現行の1次治療よりも有効であることが明らかになつつある。
そのため、胃癌においても1次治療での使用の可否を決めるための試験が進められている。
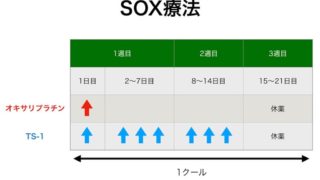
SOXまたはCapeOX+ニボルマブの臨床試験
胃癌においては、標準治療で1次治療に位置付けられているSOX療法(TS-1+オキサリプラチン)またはCapeOX療法(カペシタビン+オキサリプラチン)とニボルマブを併用する治療の効果を調べる臨床試験が進んでいる。
この結果次第で、現行の標準治療が大きく変わる可能性がある。
すでに安全性に関する結果については2017年のヨーロッパ臨床腫瘍学会(ESMO 2017)にて結果が報告されており、併用することによる副作用については想定の範囲内であると共に、腫瘍の縮小効果についても期待通りの高い効果が得られているようだ。
現在、臨床試験の最終段階である第III相試験が進められており、2019年頃には詳細な有効性が明らかになるだろう。
新たな治療法として有効性が証明されることを期待して待ちつつ、詳細なデータが発表され次第、アップデートしたいと思う。
2020年春時点におけるオプジーボの現況↓